圖(1)個股筆記:6657 華安(圖片素材取自個股官網)
更新日期:2025 年 04 月 17 日
免責聲明
請先參閱首頁的免責聲明,再繼續閱讀本文。
快速總覽
本文深入剖析華安醫學(6657)的公司概況、發展歷程、核心技術與研發策略,以及主要產品線。華安醫學以ENERGI 藥物開發平台為核心,專注於新藥研發,尤其在皮膚傷口癒合、異常性落髮和神經退化疾病領域具有顯著進展。公司近期重要事件包括 ENERGI-F705PD(巴金森氏症口服藥)獲台灣 TFDA 核准執行臨床一期試驗,以及與台灣田邊製藥和群聯電子簽署合作備忘錄,分別布局台灣及東南亞市場,並導入 AI 藥物開發技術加速藥物開發。基本面量化指標雷達圖顯示公司在股東權益報酬率、預估本益成長比、預估本益比、股價淨值比、預估殖利率等面向的分布狀況,如下圖所示:
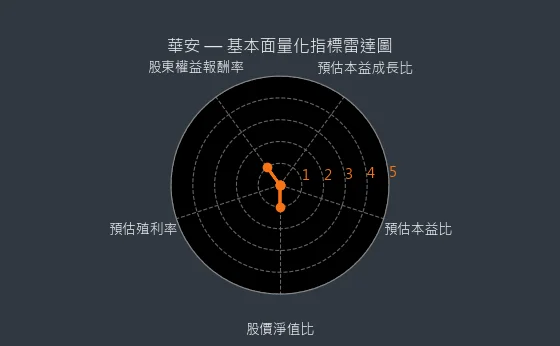
質化暨市場面分析雷達圖則揭示了公司在產業前景、題材利多、訊息多空比、法人動向等方面的市場前景,如下圖所示:
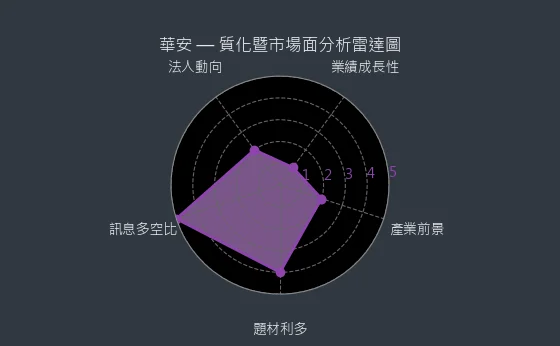
本篇文章重點在於華安醫學的 ENERGI 平台、主要臨床試驗進展(特別是F703DFU 糖尿病足潰瘍凝膠的臨床三期)、以及透過藥物重新定位和學術合作加速藥物開發的策略。
公司基本資料與發展歷程
公司概要
華安醫學股份有限公司(Energenesis Biomedical Co., Ltd.),股票代號 6657,於 2012 年 8 月 28 日在台灣創立,總部位於台北市內湖區瑞光路 583 巷 21 號 6 樓之 3。華安醫學專注於新藥研發,以其獨特的 ENERGI 藥物開發平台為核心技術,致力於開發具有多重適應症潛力的小分子創新藥物。公司於 2023 年 6 月 12 日在台灣證券交易所主板正式掛牌上市。
現任董事長為邱壬乙先生,總經理為陳翰民博士,發言人為江銘燦博士。截至 2024 年初,公司員工人數約 28 名,團隊以生醫轉譯及臨床醫學研究人才為主,包含 5 位博士及 15 位碩士,組成精實的研發核心。華安醫學以生醫智財開發為導向,目標透過技術授權金(upfront)與合作開發模式收取分潤(royalty),實現商業價值。
基本概況
華安醫學(6657)目前股價為 59.5 元,預估本益比與預估現金股利則尚未有資料。公司報表更新頻率為月報與季報。
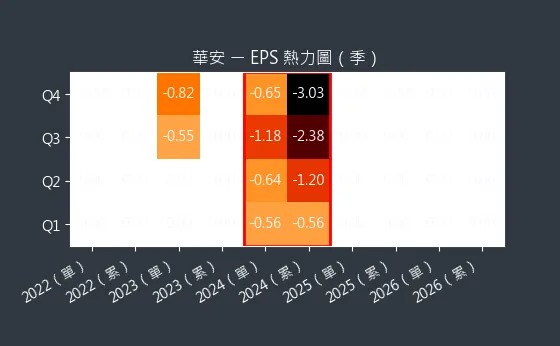
圖(2)6657 華安 EPS 熱力圖(本站自行繪製):EPS 熱力圖顯示了公司歷年 EPS 的預估變化情況。
觀察華安醫學的股價走勢,從日線圖(3)週線圖到月線圖,可看出其股價在不同時間週期的波動情況。
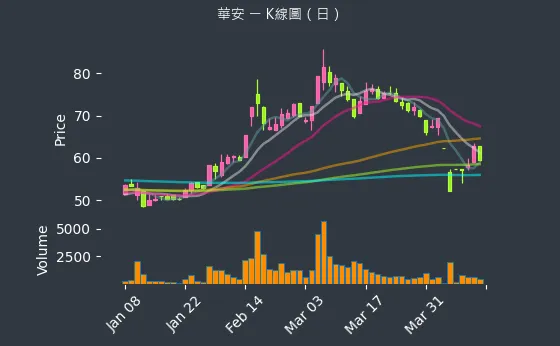
圖(4)6657 華安 K線圖(日)(本站自行繪製)
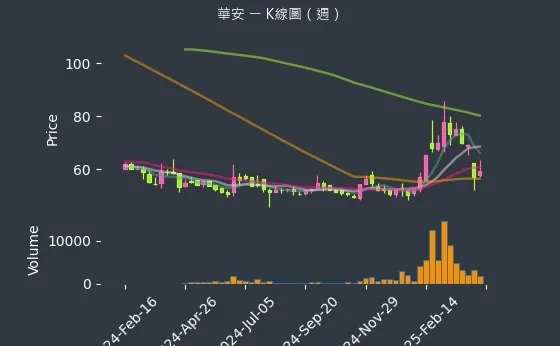
圖(5)6657 華安 K線圖(週)(本站自行繪製)
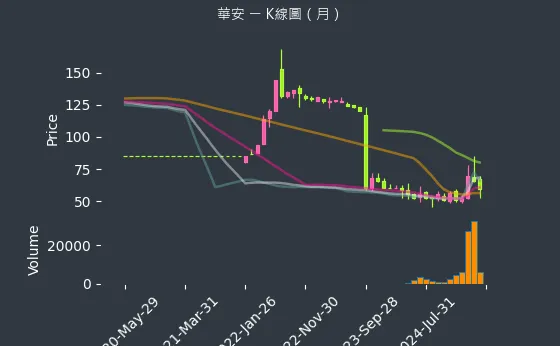
圖(6)6657 華安 K線圖(月)(本站自行繪製)
發展歷程
華安醫學自成立以來,逐步達成多項關鍵里程碑,呈現其研發能量與策略執行力:
-
2012 年:公司正式成立,並迅速獲得經濟部工業局認定為「生技新藥公司」。
-
2016 年:核心產品 ENERGI-F703DFU(糖尿病足潰瘍凝膠)獲台灣衛福部食品藥物管理署(TFDA)核准執行臨床二期試驗。
-
2017 年:獲經濟部「A+企業創新研發淬煉計畫」補助,肯定其研發潛力;同年於櫃買中心公開發行。
-
2018 年:F703DFU 臨床二期試驗開始收案;ENERGI-F701(異常性落髮外用劑)獲 TFDA 核准臨床二期試驗;同年於櫃買中心登錄興櫃。
-
2019 年:F701 臨床二期試驗開始收案;榮獲「國家新創獎」,技術創新受肯定。
-
2020 年:獲經濟部工業局出具「係屬科技事業」意見書;同年 F701 及 F703DFU 兩項臨床二期試驗成功解盲,驗證初步療效。
-
2021 年:就 F703DFU 開發進程與美國食品藥物管理局(FDA)召開 End-of-Phase 2(EOP2)會議,確立後續臨床三期方向。
-
2022 年:F703DFU 獲美國 FDA 核准執行臨床三期試驗;通過台灣證券交易所上市審議;ENERGI-F703EB(泡泡龍乳膏)取得美國 FDA 孤兒藥(Orphan Drug Designation, ODD)及罕見兒科疾病藥物(Rare Pediatric Disease Designation, RPD)認定,並獲歐盟藥品管理局(European Medicines Agency, EMA)孤兒藥認定。
-
2023 年:F703DFU 於美國與台灣同步啟動臨床三期試驗收案;公司正式於台灣證券交易所上市,邁入新的發展階段。
-
2024 年:ENERGI-F705PD(巴金森氏症口服藥)於 12 月獲台灣 TFDA 核准執行臨床一期試驗;與台灣田邊製藥於 11 月簽署 F703DFU 合作備忘錄(Memorandum of Understanding, MOU),布局台灣及東南亞市場;辦理現金增資 12,000 張,每股 48 元,預計募集 5.76 億元充實營運資金;F703EB 治療泡泡龍專利獲經濟部智慧財產局核准;以 F703DFU 獲台北生技獎創新技術獎優等獎。
-
2025 年:F705PD 於 2 月完成首位受試者收案;與瑞士 Medvisis Switzerland AG 於 3 月簽署合作備忘錄,共同拓展歐洲市場;與群聯電子於 3 月簽署合作備忘錄,導入 AI 藥物開發技術加速藥物開發。華安醫學與群聯電子簽署 MOU,合作開發 AI 藥物,將使用群聯 AI 方案,降低開發成本、加速藥物再利用,並協同陽明交大使用。華安鎖定老藥新用具優勢,AI 驅動藥物開發。華安已導入 NVIDIA 的 AI 工具,進行老藥新用新適應症探索。群聯的「aiDAPTIV+」突破記憶體限制,支持更大規模 AI 模型。群聯執行長潘健成表示將協助華安以可負擔成本訓練更大規模 AI 模型,國際機構預估 28 年全球 AI 藥物開發市場規模將達 49 億美元。
資本結構與主要股東
截至 2024 年 3 月 31 日,華安醫學額定資本額為新台幣 10 億元,實收資本額約為新台幣 7.6 億元。辦理 2024 年度現金增資後(預計募集 5.76 億元),資本額預期將進一步擴充。主要股東結構呈現多元化,經營團隊與策略性投資人持股佔比較高,詳細結構如下表所示:
| 主要股東名稱 | 持有股數(股) | 持股比例 |
|---|---|---|
| 陳翰民 | 5,967,295 | 8.28% |
| 元大商業銀行受託保管專戶 | 4,747,037 | 6.23% |
| 邱壬乙 | 4,180,786 | 5.54% |
| 三福環球股份有限公司 | 1,771,000 | 2.32% |
| 洪坤南 | 1,684,192 | 2.15% |
| 旭富製藥科技股份有限公司 | 1,602,895 | 2.10% |
| 崇裕投資股份有限公司 | 1,167,500 | 1.53% |
| 松鶴國際資本股份有限公司 | 1,000,000 | 1.31% |
| 黃錦花 | 827,000 | 1.14% |
| 林宗頤 | 700,000 | 0.92% |
| 小 計 | 23,647,705 | 31.53% |
| 其 他 | 52,576,295 | 68.47% |
| 合 計 | 76,224,000 | 100.00% |
註:基準日為 2024 年 3 月 31 日。
觀察華安醫學的籌碼動向,法人籌碼日線圖顯示了法人機構的進出情況,大戶籌碼週線圖則呈現了大戶的持股變化,而內部人持股月線圖則反映了公司內部人士的持股比例。
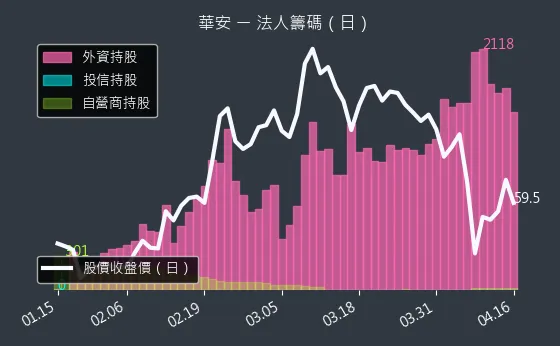
圖(7)6657 華安 法人籌碼(日)(本站自行繪製)
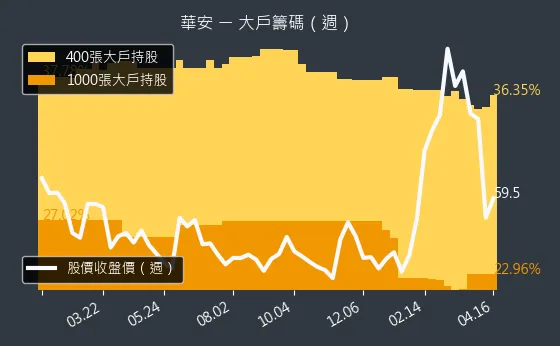
圖(8)6657 華安 大戶籌碼(週)(本站自行繪製)
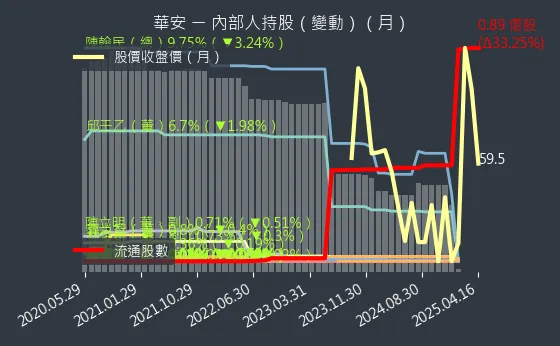
圖(9)6657 華安 內部人持股(月)(本站自行繪製)
核心技術與研發策略
ENERGI 藥物開發平台:活化細胞能量的創新機制
華安醫學的核心競爭力奠基於其獨特的 ENERGI 藥物開發平台。此平台的科學基礎在於活化細胞能量代謝的關鍵調節酵素——AMPK(AMP activated protein kinase)。透過專有的小分子藥物(分子量 MW < 250 Da)設計,目標是選擇性地調控 AMPK 活性,進而提升細胞內的能量貨幣——腺苷三磷酸(Adenosine Triphosphate, ATP)的總量。
與傳統藥物多直接作用於特定疾病靶點不同,ENERGI 平台藥物的作用機制是透過增加內源性 ATP 來強化細胞自身的細胞能量供應,促進受損或功能異常細胞的修復與調節能力,從而達到治療多種疾病的目的。由於 ATP 是生物體內固有的能量核心分子,藉由調控其濃度來治療疾病,被認為具有良好的安全性潛力,不易產生傳統小分子藥物常見的脫靶效應或副作用。此一「提升細胞能量以促進自癒」的藥物開發策略,在全球新藥研發領域具有高度創新性與獨特性。
為保護此核心技術,華安醫學已在全球主要市場(涵蓋台灣、美國、歐洲、中國、日本、韓國等)積極佈局專利組合,目前已擁有超過 30 項與 ENERGI 平台及其應用相關的核准或申請中專利,且專利組合持續擴充中,形成堅實的智慧財產權壁壘。
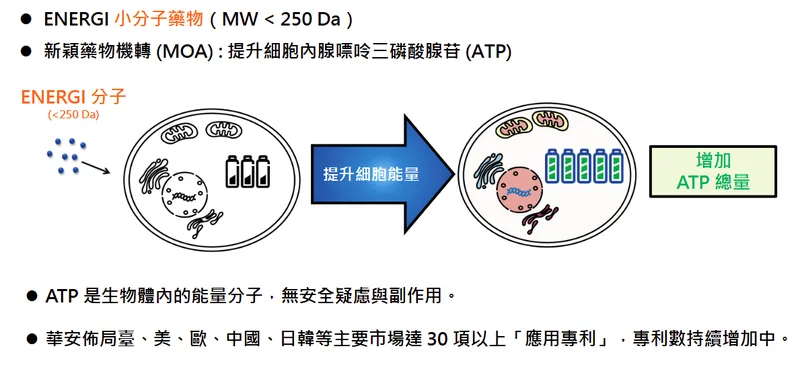
圖(10)ENERGI-藥物研發平臺(資料來源:華安醫學公司網站)
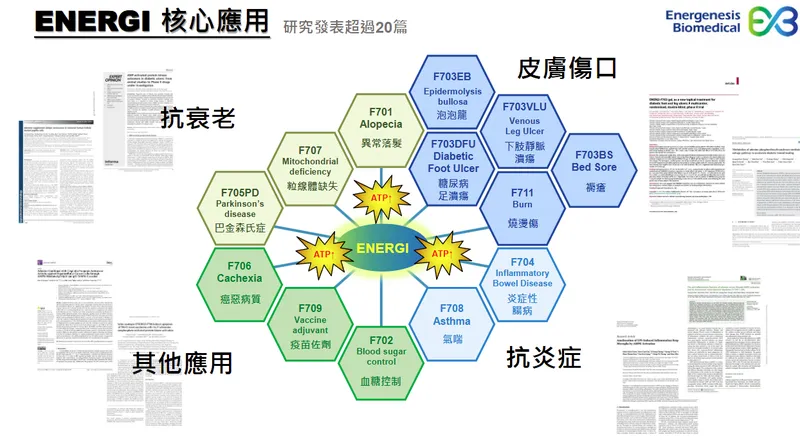
圖(11)ENERGI 核心應用顯示平台在皮膚傷口、其他應用及抗衰老上的潛力(資料來源:華安醫學公司網站)
研發策略:藥物重新定位與利基市場聚焦
華安醫學在新藥開發的主要策略上,巧妙採用了藥物重新定位(drug repositioning,亦稱老藥新用)模式,並結合美國 FDA 的 505(b)(2) 新藥申請路徑,專注於探索既有藥物分子在新適應症上的治療潛力。此策略具備多重優勢:
-
降低開發風險:選用已知安全性、藥物動力學及部分藥理毒理數據的既有藥物分子,可明顯縮短早期研發時程,並降低臨床前及早期臨床試驗的失敗風險。
-
加速開發進程:根據 505(b)(2) 路徑規定,可引用原廠藥物的公開文獻或安全性數據,簡化部分臨床前試驗要求,從而加速藥物進入人體臨床試驗的階段。
-
聚焦利基市場:策略性地鎖定「尚無有效治療藥物」或「現有療法效果有限,醫療需求未被滿足」的疾病領域,例如慢性傷口癒合(糖尿病足潰瘍、下肢靜脈潰瘍)、罕見疾病(泡泡龍症)、以及特定神經退化疾病(巴金森氏症)等。此策略有助於避開競爭激烈的紅海市場(如部分癌症領域),提升產品成功上市後的市場獨特性與商業價值。
學術合作與 AI 技術應用
為加速驗證 ENERGI 平台的廣泛治療潛力並拓展新的適應症可能性,華安醫學積極與國內外頂尖大學及研究機構展開學術合作。過去 3 年內已執行超過 30 件學術合作案。研究範疇廣泛,涵蓋神經退化疾病(巴金森氏症、阿茲海默症、路易氏體失智症)、精神相關疾病(自閉症、創傷後壓力症候群、失眠、癲癇)、糖尿病及其併發症、癌症與惡病質、乾眼症、發炎性腸道疾病、腎損傷、肌肉萎縮症等多個面向。
這些合作不僅加速了早期探索,其研究成果也陸續發表於 20 多篇具影響力的國際學術期刊(例如 EClinicalMedicine, FASEB J 等),從科學角度驗證了 ENERGI 平台在多種疾病動物模型上的潛在療效。
近年來,面對全球藥物開發導入人工智慧(Artificial Intelligence, AI)的趨勢,華安亦積極擁抱新技術。2025 年 3 月,公司宣布與全球知名的快閃記憶體控制晶片暨儲存解決方案領導者——群聯電子 簽署合作備忘錄。合作內容將採用群聯專為生成式 AI 模型訓練所設計的 aiDAPTIV+ AI 平台。該平台透過軟硬體整合,能有效突破現有 GPU 記憶體容量的限制,支援更大規模的 AI 模型訓練。華安醫學將藉此平台,結合其累積的藥物數據與陽明交通大學等學術夥伴的研究能量,透過大數據分析與深度學習演算法,加速探索 ENERGI 小分子藥物的新穎藥理機制、預測潛在新適應症、優化藥物設計,預期能明顯提升研發效率、降低開發成本,並提高新藥開發的成功機率。華安亦已導入 NVIDIA 的 AI 工具進行老藥新用新適應症探索。
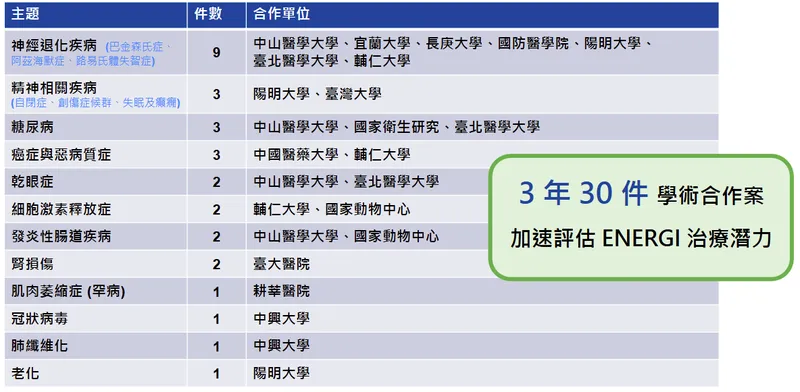
圖(12)擴大學術合作加速新藥開發,過去三年已執行 30 件(資料來源:華安醫學公司網站)
學術合作概況 (近 3 年)
| 主題 | 件數 | 合作單位 |
|---|---|---|
| 神經退化疾病 (巴金森氏症、阿茲海默症、路易氏體失智症) | 9 | 中山醫學大學、宜蘭大學、長庚大學、國防醫學院、陽明交通大學、臺北醫學大學、輔仁大學 |
| 精神相關疾病 (自閉症、創傷症候群、失眠及癲癇) | 3 | 陽明交通大學、臺灣大學 |
| 糖尿病 | 3 | 中山醫學大學、國家衛生研究院、臺北醫學大學 |
| 癌症與惡病質 | 3 | 中國醫藥大學、輔仁大學 |
| 乾眼症 | 2 | 中山醫學大學、臺北醫學大學 |
| 細胞激素釋放症 | 2 | 輔仁大學、國家動物中心 |
| 發炎性腸道疾病 | 2 | 中山醫學大學、國家動物中心 |
| 腎損傷 | 2 | 臺大醫院 |
| 肌肉萎縮症 (罕見疾病) | 1 | 耕莘醫院 |
| 冠狀病毒 | 1 | 中興大學 |
| 肺纖維化 | 1 | 中興大學 |
主要研發專案與產品線
華安醫學運用其核心 ENERGI 平台,已成功發展出多個進入不同臨床或臨床前階段的候選藥物。這些產品線涵蓋皮膚科(傷口癒合、落髮)、神經科(神經退化疾病)、代謝疾病、以及炎症相關疾病等多個治療領域,呈現平台的廣泛應用潛力。
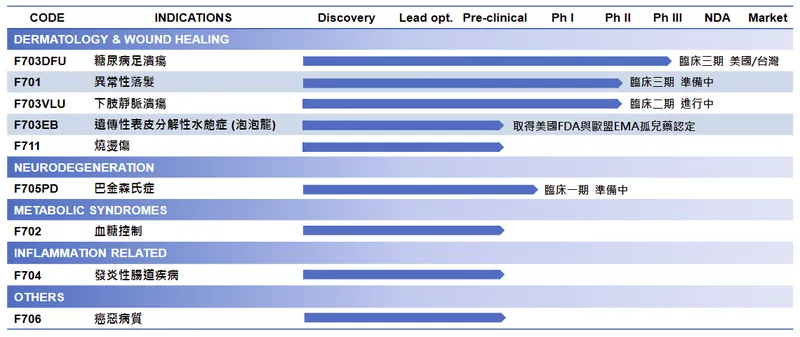
圖(13)ENERGI 研發專案涵蓋多個治療領域(資料來源:華安醫學公司網站)
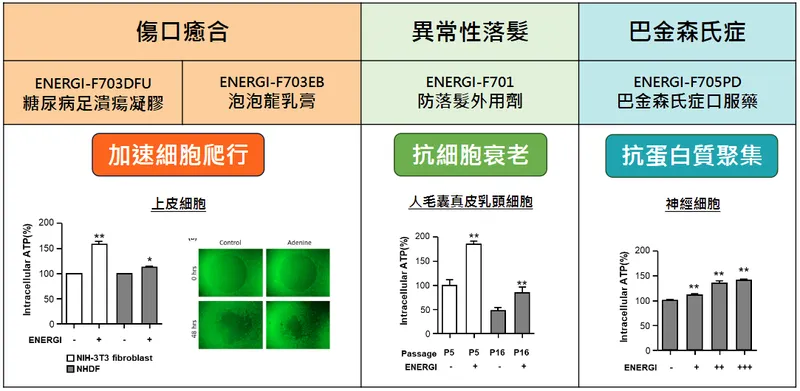
圖(14)三大主要臨床試驗:傷口癒合、異常性落髮、巴金森氏症(資料來源:華安醫學公司網站)
皮膚傷口癒合領域
此領域是華安目前臨床進展最快的重點項目,利用 ENERGI 平台促進細胞能量代謝,加速皮膚修復。
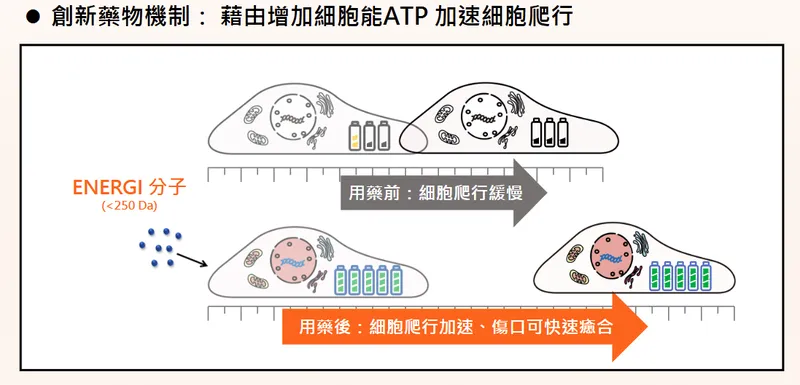
圖(15)ENERGI 藥物透過增加細胞能量 ATP 加速細胞爬行,促進癒合(資料來源:華安醫學公司網站)
ENERGI-F703DFU:糖尿病足潰瘍外用凝膠
-
適應症:糖尿病足部潰瘍(Diabetic Foot Ulcer, DFU)。此為糖尿病常見且嚴重的併發症。全球約有 5.4 億 糖尿病患者,其中高達 34% 的患者在其一生中可能發生足部潰瘍。DFU 不僅癒合困難,易反覆感染,嚴重時甚至需要截肢(2.9% DFU 患者需截肢),造成巨大的醫療負擔與生活品質下降,存在迫切且未被滿足的醫療需求。
-
作用機制:ENERGI 分子透過提升傷口周邊皮膚細胞(特別是角質細胞與纖維母細胞)的 ATP 含量,活化細胞能量代謝,促進細胞爬行、增生與分化,從而加速上皮化過程,達到促進傷口癒合的目的。此機制與傳統生長因子或清創藥物不同。
-
市場現況與競爭:
- 全球困難傷口治療市場 2024 年約 81 億美元,預計 2033 年將增長至 121 億美元。其中北美市場最大。
- 目前美國 FDA 僅核准一款 DFU 外用生物製劑——Regranex® (Smith & Nephew),但其價格高昂(1,400 美元/15g),且仿單建議主要用於 5 cm² 以下的傷口,對於較大面積或複雜傷口效果受限,導致其全球市佔率低於 1%。
- 台灣本土研發的植物新藥 ON101(速必一®) (合一藥品) 已在台灣上市,提供另一種治療選擇。
- ENERGI-F703DFU 作為小分子藥物,預期生產成本相對較低(預估 250~300 美元/25g),且臨床二期數據顯示對不同大小的 DFU 均可能有效(包括 23.5 cm² 大型傷口也能在 16 週癒合),具備潛在的市場競爭優勢。
-
臨床進展:
- 臨床二期試驗:在台灣執行的多中心、隨機、雙盲試驗結果亮眼。主要療效指標顯示,在 12 週的治療期程中,使用 F703DFU 凝膠組的傷口完全癒合率顯著優於安慰劑組(ITT 分析:43.9% vs 10.0%, P<0.05;PP 分析:36.7% vs 9.1%, P<0.05)。此試驗成果已於 2022 年發表在國際知名醫學期刊 EClinicalMedicine。
- 臨床三期試驗:基於二期正向結果,目前正在美國與台灣同步進行關鍵性臨床三期試驗,目標美國收案人數約 230 人及相應數量的台灣受試者。收案進展順利,預計 2025 年底 可完成所有受試者收案,並進行數據解盲。公司表示,若數據良好,不排除提前解盲的可能性。
- 歐洲臨床規劃:已規劃於 2025 年第三季向歐洲藥品管理局(EMA)遞交臨床試驗申請,預計收案人數約 230 人,啟動歐洲地區的臨床三期試驗。
-
預期取證時程:根據目前進度推估,若三期臨床數據成功,預計 2026 年首先在台灣申請藥證;美國藥證預計於 2026 年至 2027 年間取得;歐洲藥證則預計在 2027 年取得。
-
商業合作:已與台灣田邊製藥簽署合作備忘錄(MOU),布局台灣及東南亞市場。將與日本田邊三菱製藥簽訂授權銷售與製造合約。歐美市場授權洽談接近尾聲,解盲成功後有機會敲定合約。

圖(16)糖尿病足潰瘍市場規模龐大,現有療法市佔率低(資料來源:華安醫學公司網站)
F703DFU 凝膠與現有療法比較
| ENERGI-F703DFU 凝膠 | Regranex® 凝膠 | ON101 乳膏 (速必一®) | |
|---|---|---|---|
| 藥物分類 | 小分子藥物 | 生物製劑(大分子藥物) | 植物藥 |
| 活性成分 | ENERGI | 重組人類血小板衍生 生長因子 | 左手香與積雪草 萃取物 |
| 用藥途徑 | 皮膚外用 | 皮膚外用 | 皮膚外用 |
| 開發階段 | 美國與台灣臨床三期 執行中 | FDA 核准上市 | TFDA 核准上市 |
| 價格 | 預計 250~300 USD/25 g | 1,400 USD/15g | 9,800 NTD/15g |
ENERGI-F703EB:遺傳性表皮分解性水皰症 (泡泡龍) 乳膏
-
適應症:遺傳性表皮分解性水皰症(Epidermolysis Bullosa, EB),俗稱「泡泡龍症」。此為一種罕見且嚴重的遺傳性皮膚疾病,患者皮膚極度脆弱,輕微摩擦即可能產生水泡或破皮。
-
市場潛力與現行療法:全球 EB 患者估計超過 50 萬人,市場規模約 24 億美元 (2023)。美國、歐洲七大主要市場(7MM)患者約 4.65 萬人,市場規模約 13 億美元。現行治療多以症狀控制為主。近期雖有基因療法 Krystal’s VYJUVEK (用於 DEB,年費用 63 萬美元) 和 Chiesi 公司的 Filsuvez® (用於 DEB/JEB) 核准,但 F703EB 預計可應用於所有 EB 類型,作為加速傷口癒合的第一線療法,市場定位清晰。
-
特殊資格認定:F703EB 已成功取得 美國 FDA 的孤兒藥資格(ODD)及罕見兒科疾病認定(RPD),同時也獲得 歐盟 EMA 的孤兒藥資格(ODD)。這些資格有助於加速藥物審查並提供市場獨佔期。
-
臨床進展:目前處於臨床二期試驗的準備階段。
其他皮膚傷口相關產品線(如 F703VLU 下肢靜脈潰瘍 – 臨床二期進行中、F703BS 褥瘡 – 臨床前、F711 燒燙傷 – 臨床一期準備中)亦在早期開發階段,利用相似機制拓展應用範圍。

圖(17)泡泡龍症市場與 F703EB 的潛在定位(資料來源:華安醫學公司網站)
異常性落髮領域
此領域利用 ENERGI 平台抗細胞老化的潛力,開發非傳統機轉的落髮治療方案。
ENERGI-F701:防落髮外用劑
-
適應症:異常性落髮,包含男性雄性禿(Androgenetic Alopecia, AGA)及女性型態落髮。
-
作用機制:ENERGI 分子透過提高毛囊真皮乳頭細胞的 ATP,抵抗細胞老化壓力,可能藉此延緩毛囊萎縮,維持正常的毛髮生長週期,達到抗落髮的效果。
-
市場現況與競爭:
- 全球落髮治療市場規模預計從 2023 年的 33 億美元成長至 2030 年的 58 億美元。現有主要藥物為 Minoxidil (落建) 及 Finasteride (柔沛)。Minoxidil 促生髮效果為主,Finasteride 僅適用男性且有潛在性功能副作用。市場缺乏能快速有效防止落髮,且男女適用的新藥。
- ENERGI-F701 臨床二期數據顯示其具備快速防止落髮(女性用藥 4 週落髮量降至 60%,優於落建需 12 週)的潛力,且男女皆可使用,無傳統藥物副作用,具備市場區隔潛力,特別是在服務未被滿足的女性落髮市場。
-
臨床進展:
- 臨床二期試驗(男性 AGA):結果顯示,使用 F701 兩個月後,醫師評估改善率達 75%,顯著優於安慰劑組(80% 為相同或較差)。
- 臨床二期試驗(女性落髮):數據顯示,使用 F701 僅需 4 週即可將落髮量降低約 40% (達到正常落髮範圍的 60%),效果顯著快於對照組 Minoxidil (需 12 週)。
- 後續規劃:目前正處於臨床三期試驗的準備階段,預計將申請多國臨床試驗,並可能探索非處方藥(Over-The-Counter, OTC)或化妝品通路的可能性,加速產品上市。2025 年內有望進入商業化階段。
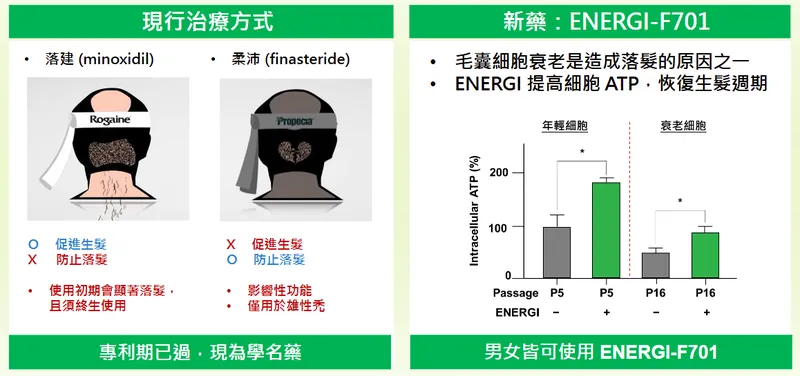
圖(18)ENERGI-F701 的市場定位與臨床二期數據亮點(資料來源:華安醫學公司網站)
神經退化疾病領域
此為華安新拓展的重點領域,利用 ENERGI 平台調節神經細胞能量與蛋白質穩態的潛力,開發創新療法。
ENERGI-F705PD:巴金森氏症口服藥
-
適應症:巴金森氏症(Parkinson’s Disease, PD)。PD 是僅次於阿茲海默症的第二大神經退化性疾病,全球患者超過 1,000 萬人。主要病理特徵為中腦黑質多巴胺神經元退化及腦內 α-突觸核蛋白 (α-synuclein) 的異常聚集。
-
作用機制:F705PD 採用創新的「抗 α-突觸核蛋白聚集」策略。臨床前研究發現,ENERGI 分子不僅能增加神經細胞能量,其提升的 ATP 還可能扮演生物性助溶劑的角色(馬克斯·普朗克研究所證實),有助於溶解或抑制 α-synuclein 等易聚集蛋白質的不正常堆積,從根本上延緩或阻止疾病進程。動物實驗亦顯示 F705PD 能改善巴金森氏症模型小鼠的運動能力,呈現具有反轉 PD 症狀的潛力。此機制為全球首創。
-
市場現況與競爭:
- 全球 PD 治療市場規模 2022 年約 58.7 億美元(其中 Carbidopa-levodopa 銷售達 17 億美元),預計 2030 年將成長至 121.5 億美元。現行療法多以補充多巴胺或延緩其分解為主,僅能緩解症狀,無法阻止疾病惡化。
- ENERGI-F705PD 提供了一種針對疾病根源的潛在新療法,若臨床證實有效,將填補目前治療的巨大空白,市場潛力龐大。
-
臨床進展:
- 臨床一期試驗:已於 2024 年 12 月獲台灣 TFDA 核准執行,並於 2025 年 2 月在台北醫學大學附設醫院完成首位受試者收案。此試驗主要評估藥物在健康受試者中的安全性與耐受性,預計招收 24 名參與者,力拚 2025 年第二季完成。
- 後續規劃:取得一期臨床數據後,規劃向美國 FDA 申請臨床二期試驗,進一步評估在 PD 患者身上的療效。
其他產品線如 F702(血糖控制)、F704(發炎性腸道疾病)、F706(癌惡病質)、F707(粒線體缺失)、F708(氣喘)、F709(疫苗佐劑)等,目前多處於臨床前探索或早期研究階段,是 ENERGI 平台未來潛在的應用方向。

圖(19)ENERGI-F705PD 採用抗蛋白質聚集的創新機制(資料來源:華安醫學公司網站)
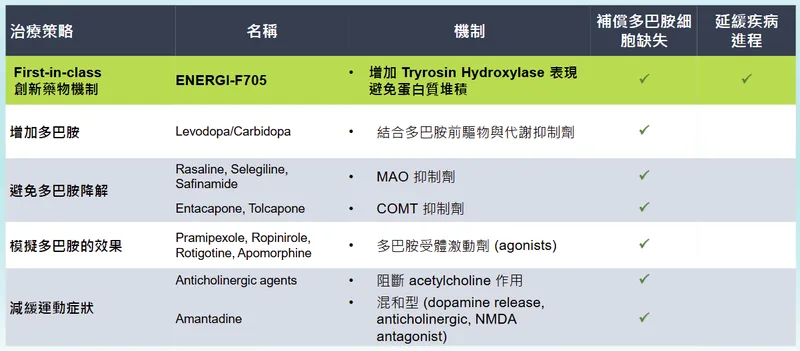
圖(20)現有巴金森氏症療法與 ENERGI-F705PD 的機制比較(資料來源:華安醫學公司網站)
市場分析與營運概況
營收結構與來源
截至 2024 年底,華安醫學仍處於新藥研發的關鍵投入階段,尚未有任何新藥產品正式上市貢獻營收。2024 年全年營收約 774.9 萬新台幣。公司目前的營業收入主要來自兩部分:
-
試劑產品銷售:透過自有品牌 “Visual Protein” 及代理國際品牌,銷售生命科學研究相關的實驗試劑,約佔 53%。主要供應商包括永傑生物科技、鴻林堂生物科技、景明化工、波仕特生物科技等。
-
檢測分析服務:提供委託研究或檢測服務,約佔 47%。
2025 年 3 月單月營收為 48.6 萬新台幣,年減 35.29%,月增 64.75%,顯示營收仍有波動。公司預計未來主要的營運及獲利來源將是新藥技術授權金(upfront)與上市後的分潤收入(royalty)。
區域市場分析
根據 2023 年資料,華安醫學的銷售區域以台灣內銷為主,約佔 80%,外銷約佔 20%。外銷市場初期涵蓋東南亞地區,未來隨著 F703DFU 等產品的國際授權與臨床推進,預計歐洲、美國及中東市場的營收比重將明顯提升。
客戶群體分析
目前主要客戶包括生命科學研究領域的學術單位、公私立大學、教學醫院及生技公司,這些客戶主要購買公司的試劑產品及檢測分析服務。未來隨著新藥上市,客戶群將擴大至全球醫療機構、藥廠及醫療服務商。
生產與供應鏈
華安醫學主要生產基地位於台北總部,用於試劑產品研發與品管。新藥生產則採委外合作模式,與國內外具備 GMP 認證的委託生產機構(Contract Manufacturing Organization, CMO)合作,如旭富製藥、寶齡富錦生技、中生生技製藥等,負責原料藥與成品生產。此策略降低了初期資本投入與生產風險。
- 原物料:試劑與新藥研發需依賴國內外供應商提供生物活性物質、化學品、酶等。全球生技原料市場供應相對緊張,可能影響成本與交期。公司透過長期合約與多元供應商管理來應對。
- 產能規劃:目前產能配合臨床試驗需求。未來 F703DFU 等產品若成功商業化,預計將與合作夥伴擴大產能,甚至可能建立自有或專屬生產線,以滿足市場需求。
競爭優勢與市場地位
競爭態勢分析
華安醫學在各產品領域面臨不同的競爭對手:
- 糖尿病足潰瘍:主要競爭者為 Smith & Nephew (Regranex®)、合一藥品 (ON101)、Daewoong Pharmaceutical (Easyef) 及其他開發中藥物廠商。
- 異常性落髮:主要競爭者為 Johnson & Johnson (Rogaine®)、Merck (Propecia®)。
- 巴金森氏症:主要競爭者為大型國際藥廠,開發補充多巴胺或抑制其降解的藥物。
華安的利基市場策略使其在特定領域(如創新機制、罕見病)能避開部分直接競爭。
核心競爭力
- 獨特技術平台:ENERGI 平台為全球首創以 ATP 提升促進細胞自癒的機制,具備多適應症潛力與良好安全性。
- AI 輔助藥物開發:與群聯電子等合作,導入 AI 技術加速研發,提升效率與成功率,降低成本。
- 專利佈局:在全球主要市場擁有 30 項以上應用專利,且持續增加,構築技術壁壘。
- 聚焦未滿足需求:專注於 DFU、PD、EB 等尚無有效療法或現有療法效果有限的利基市場。
- 國際合作網絡:與台灣田邊、瑞士 Medvisis 等建立合作關係,加速國際市場拓展。
市場地位
目前華安醫學仍是研發階段公司,在整體醫藥市場尚未建立顯著市佔率。然而,其在糖尿病足潰瘍、巴金森氏症等領域的創新療法已使其成為備受矚目的生技新藥概念股,具備成為利基市場領導者的潛力。
近期重大事件分析
- 2025.03:與瑞士 Medvisis 簽署 MOU,合作拓展歐洲市場,推動 F703DFU、F703VLU、F701 歐洲三期臨床與商業化。
- 2025.03:與群聯電子簽署 MOU,導入 aiDAPTIV+ AI 平台,加速 AI 藥物開發。
- 2025.02:ENERGI-F705PD 巴金森氏症口服藥完成首位受試者收案,一期臨床試驗正式啟動。
- 2025.02:現金增資股上市交易,股價表現強勁,創一年新高,法人連續買超。
- 2025.02:獲納入臺灣指數公司生技醫療股價指數成分股。
- 2024.12:ENERGI-F705PD 獲 TFDA 核准執行一期臨床試驗。
- 2024.12:公告辦理現金增資 1.2 萬張,每股 48 元,募集 5.76 億元。
- 2024.11:與台灣田邊製藥簽署 F703DFU 合作 MOU。
未來發展策略展望
短期發展計畫(1-2 年)
- 臨床試驗推進:完成 F703DFU 美國/台灣三期臨床試驗收案與解盲;啟動 F703DFU 歐洲三期臨床;完成 F705PD 一期臨床試驗並準備進入二期;推進 F701 三期臨床準備。
- 國際授權合作:完成 F703DFU 歐美市場的授權洽談;落實與日本田邊三菱、瑞士 Medvisis 的合作細節。
- AI 平台應用深化:利用與群聯合作的 AI 平台,加速新適應症探索與早期藥物開發。
- 資金規劃:確保現金增資募集資金到位,支持各項臨床試驗與營運需求。
中長期發展藍圖(3-5 年)
- 產品上市與商業化:力拚 F703DFU 在台灣、美國、歐洲等地成功取得藥證並上市銷售;推動 F701、F705PD 等後續產品進入市場。
- 擴大產品線:基於 ENERGI 平台,持續開發其他適應症新藥,如 F703EB、F703VLU、F702、F704 等。
- 全球市場滲透:透過授權合作與自建通路,逐步擴大全球市場版圖。
- 產能建置:視商業化需求,與合作夥伴擴大產能,或評估建立自有生產設施。
- 持續研發創新:利用 AI 等先進技術,不斷優化 ENERGI 平台,探索新藥物靶點與機制。
投資價值綜合評估
投資亮點
- 創新技術平台:ENERGI 平台具獨特性與多適應症潛力,提供差異化競爭優勢。
- 產品線佈局:聚焦未滿足醫療需求的利基市場,如 DFU、PD 等,市場潛力龐大。
- 臨床進展明確:核心產品 F703DFU 已進入關鍵三期臨床,接近收成期。F705PD、F701 亦有明確進展。
- AI 技術加持:導入 AI 提升研發效率,符合產業趨勢。
- 國際合作積極:與多家國際夥伴合作,加速全球市場佈局。
面臨風險
- 臨床試驗不確定性:新藥開發 inherently 存在失敗風險,臨床結果不如預期將嚴重影響公司價值。
- 資金需求壓力:研發投入巨大,未來仍需持續融資或依賴授權金支持營運。
- 市場競爭激烈:各領域均有大型藥廠競爭,產品上市後仍需面對市場推廣挑戰。
- 法規審批風險:各國藥監機構審批標準與時程不同,可能影響上市進度。
- 商業化能力考驗:從研發走向商業化需要建立銷售、行銷、生產等不同能力。
投資人參考要點
投資華安醫學需密切關注其臨床試驗數據的發布(尤其是 F703DFU 的三期解盲結果)、國際授權合約的簽訂進度、F705PD 等後續產品的臨床發展、以及公司資金狀況與未來融資計畫。雖然公司目前尚未盈利且風險較高,但其創新技術與市場潛力使其具備高成長的想像空間,適合風險承受度較高的投資人。
重點整理
- 核心技術:獨特的 ENERGI 藥物平台,透過提升細胞 ATP 促進自癒。
- 研發策略:藥物重新定位(老藥新用)+ 505(b)(2) 路徑,聚焦未滿足醫療需求的利基市場。
- 重點產品線:
- F703DFU (糖尿病足潰瘍):美/台三期臨床中,預計 2025 年底解盲,歐洲三期 Q3 2025 啟動。
- F701 (異常性落髮):二期完成,準備三期,具快速防落髮優勢。
- F705PD (巴金森氏症):一期臨床進行中,創新抗蛋白質聚集機制。
- F703EB (泡泡龍):獲美歐孤兒藥資格,準備二期。
- AI 應用:與群聯電子合作導入 AI 平台,加速藥物開發。
- 國際合作:與台灣田邊、瑞士 Medvisis 合作,積極拓展亞太與歐洲市場,歐美授權洽談中。
- 財務狀況:研發投入期,尚未盈利,依賴現金增資與未來授權金。
- 市場潛力:各產品線目標市場規模龐大,若成功上市具高成長潛力。
- 主要風險:臨床失敗、資金需求、市場競爭、法規審批。
參考資料說明
公司官方文件
-
華安醫學股份有限公司 法人說明會簡報 (2024.04.11)
此份簡報為本研究提供了公司概況、發展歷程、資本結構、ENERGI 平台技術細節、主要研發專案進度(含 F703DFU、F701、F703EB、F705PD)、臨床試驗數據、市場分析及未來展望等核心資訊。 -
華安醫學股份有限公司 2024 年度現金增資公開說明書 (2024.12)
此文件說明了現金增資計畫的細節、資金用途(主要為新藥研發與臨床試驗)及公司當時的財務與營運狀況。 -
華安醫學股份有限公司 歷次重大訊息公告 (2024-2025)
相關公告提供了 F705PD 臨床試驗核准與收案、與台灣田邊/瑞士 Medvisis/群聯電子簽署 MOU、現金增資股上市、納入指數成分股等最新事件資訊。
研究報告
-
券商研究報告 (例如:元大證券、富邦證券等,日期約 2024-2025)
此類報告提供了對華安醫學技術平台、產品線潛力、市場競爭格局及財務預測的獨立分析與評價。 -
產業分析機構報告 (例如:環球生技月刊、GBI MONTHLY 等,日期約 2024-2025)
提供了產業趨勢分析、AI 藥物開發動態、以及法人對華安醫學的持股與評價資訊。
新聞報導
-
財經媒體報導 (例如:鉅亨網、經濟日報、工商時報、MoneyDJ 等,日期約 2024-2025)
報導了公司法說會內容、重大合作案宣布、股價異動、臨床試驗進展等即時新聞。 -
科技媒體報導 (例如:科技新報、聯合新聞網 udn 等,日期約 2025)
著重報導了華安醫學與群聯電子的 AI 合作細節及其在 AI 藥物開發領域的布局。
網站資料
-
華安醫學官方網站 (energenesis-biomedical.com)
提供了公司基本介紹、技術平台說明、產品線資訊、新聞發布等官方資訊。 -
公開資訊觀測站 (mops.twse.com.tw)
提供了公司財務報表、股東會與董事會決議、重大訊息等法定公開資訊。 -
財經資訊平台 (例如:Yahoo 股市、財報狗 Statementdog、Goodinfo! 等)
提供了股價、營收、財務比率、法人持股等即時數據與歷史資料。
