圖(1)個股筆記:6492 生華科(圖片素材取自個股官網)
更新日期:2025 年 05 月 19 日
免責聲明
請先參閱首頁的免責聲明,再繼續閱讀本文。
快速總覽
本文深入解析生華生物科技股份有限公司(6492.TWO),一家專注於小分子抗癌新藥及特殊原料藥開發的台灣生技公司。本篇文章重點涵蓋公司基本資料、發展歷程、經營團隊、核心產品與技術平台、研發管線、產品應用領域與市場潛力、營運與財務概況、市場布局與競爭分析、近期重大事件與進展,以及未來發展策略與展望。
從基本面量化指標雷達圖來看,生華科在股東權益報酬率、預估本益成長比、預估本益比、股價淨值比、預估殖利率等方面有其獨特分佈,需要進一步分析其基本面健康狀況。

圖(2)6492 生華科 基本面量化指標雷達圖(本站自行繪製)
而從質化暨市場面分析雷達圖來看,產業前景、題材利多、訊息多空比、法人動向等因素交織,影響著公司的市場前景。
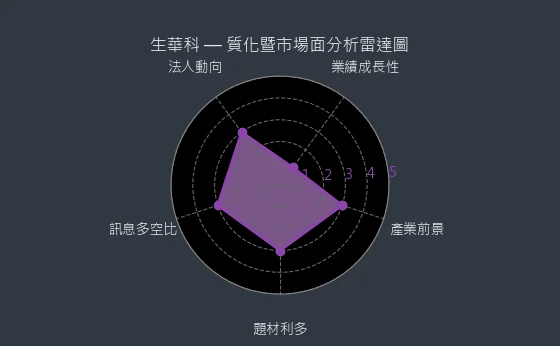
圖(3)6492 生華科 質化暨市場面分析雷達圖(本站自行繪製)
公司重要事件包含:CX-5461 獲 NCI NExT 計畫贊助、ESMO 年會發表臨床試驗結果;CX-4945 基底細胞癌數據正向、兒科腫瘤臨床試驗啟動、神經母細胞瘤孤兒藥認定、社區型肺炎試驗終止;延攬馮玉蓮博士加入團隊。
整體而言,生華科具備創新研發能力和國際合作優勢,但在財務表現上仍面臨挑戰。未來發展策略將聚焦核心產品、拓展免疫療法、深化精準醫療,並積極尋求國際授權與合作。
生華生物科技股份有限公司(Senhwa Biosciences, Inc.,股票代號:6492.TWO)於 2012 年 11 月 16 日在新北市新店區成立,專注於開發具備新穎作用機制的小分子抗癌新藥及特殊原料藥。公司以「創新帶來美好生活」為企業理念,致力於透過技術創新,研發有效對抗癌症並改善人類健康之藥物,並以成為 First-in-class 新藥開發公司為目標。
公司基本資料
| 項目 | 內容 |
|---|---|
| 公司名稱 | 生華生物科技股份有限公司 |
| 英文名稱 | Senhwa Biosciences, Inc. |
| 股票代號 | 6492.TWO |
| 成立時間 | 2012 年 11 月 16 日 |
| 公司地址 | 新北市新店區北新路 3 段 225 號 10 樓 |
| 董事長 | 胡定吾 |
| 總經理 | 黃品諺 (代理) |
| 發言人 | 張小萍 |
| 實收資本額 | 新台幣 897,443,920 元 (截至 2024 年底) |
| 掛牌上櫃日期 | 2017 年 4 月 24 日 |
| 員工人數 | (未提供) |
| 主要業務 | 抗癌新藥及特殊原料藥研發 |
| 官方網站 | https://www.senhwabio.com/tw |
公司基本概況
生華科(6492.TWO)目前股價約為 33.4 元。圖(4)6492 生華科 EPS 熱力圖顯示歷年 EPS 預估變化。
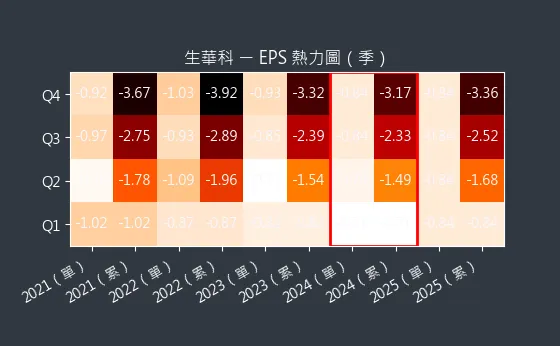
圖(5)6492 生華科 EPS 熱力圖(本站自行繪製)
圖(6)6492 生華科 K 線圖(日)、(週)、(月)分別呈現了近期的股價走勢,投資者可藉此觀察股價的短期、中期與長期變化。
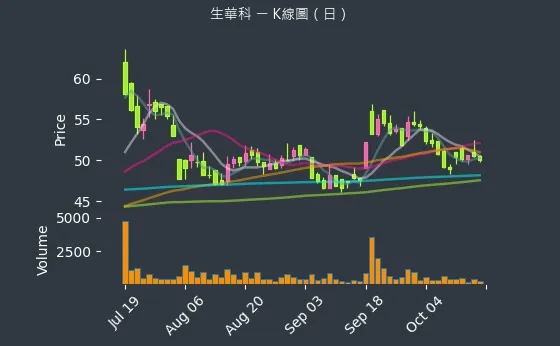
圖(7)6492 生華科 K線圖(日)(本站自行繪製)
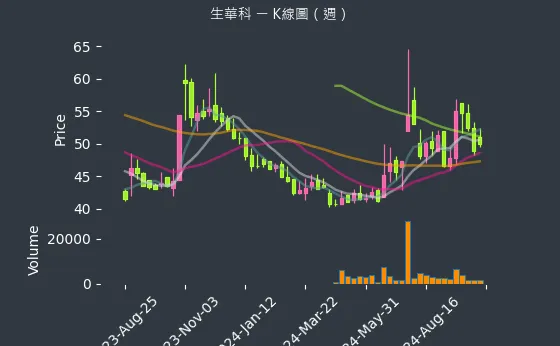
圖(8)6492 生華科 K線圖(週)(本站自行繪製)
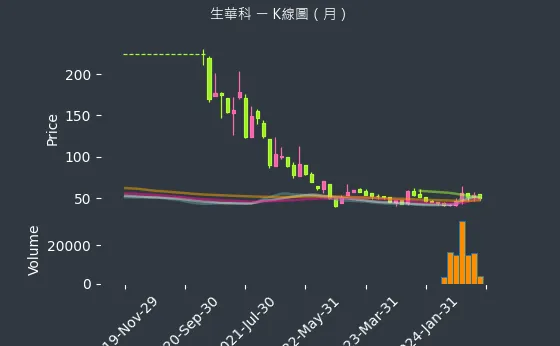
圖(9)6492 生華科 K線圖(月)(本站自行繪製)
發展歷程與轉型
奠基與轉型 (2012-2017)
生華科創立初期,即確立以小分子抗癌新藥開發為核心方向,並採取臨床開發為主、基礎研究為輔的策略。公司結合標靶藥物與組合療法,目標開發具創新機制之新型抗癌藥物,期望在競爭激烈的生技產業中快速取得進展。
資本市場與國際拓展 (2017-至今)
2017 年 4 月 24 日,生華科於證券櫃檯買賣中心 (TPEx) 成功上櫃,為公司發展注入資本動能。上櫃後,生華科加速研發進程,積極尋求國際合作,如 2015 年被選為加拿大 SU2C-CBCF「抗乳癌夢幻團隊」成員,獲得 九百萬加幣研究經費支持,並持續拓展全球市場。
經營團隊
生華科經營團隊匯集多位具備國際藥廠經驗之資深專家,為公司發展提供堅實後盾:
-
胡定吾:現任董事長。
-
黃品諺醫師:現任代理總經理,畢業於臺北醫學大學醫學系,並取得東吳大學法律碩士,兼具醫學專業與法律背景。
-
馮玉蓮博士 (法人董事代表,2024 年 11 月延攬):具備近 30 年國際藥廠新藥研發經驗,曾任嬌生集團楊森藥廠全球總裁、諾華癌症事業部執行長等要職,並擔任科技部特聘顧問及行政院生技產業策略諮議委員會 (BTC) 委員。其於臨床生物標誌、診斷策略及精準醫療領域具備深厚專業,預期能加速公司國際商業化進程。生華科於 2024 年 11 月延攬馮玉蓮博士擔任法人董事代表,強化經營團隊專業能力。
-
陳敏鋑醫師:現任美國 MultiCare Regional Cancer Center 資深醫師及華盛頓大學醫學中心 (UW MED) 臨床教師,具備豐富臨床腫瘤學經驗。
-
張小萍:現任發言人。
核心產品與技術平台
生華科聚焦於小分子抗癌新藥開發,目前主要產品線包含兩大核心藥物:
CX-5461 (Pidnarulex):RNA 聚合酶 I 抑制劑
CX-5461 為 First-in-class 的 RNA 聚合酶 I 抑制劑,也是全球首個臨床運用 G-四鏈體 (G-quadruplex) 結構作用機制的抗癌藥物。其作用機制獨特,能選擇性活化抑癌蛋白 p53,並具備 DNA 損傷修復(DDR)抑制機制,針對癌細胞進行精準打擊,同時降低對健康細胞之影響。Pidnarulex 優先鎖定血液性癌症 (如血癌] 及帶有 BRCA2/PALB2 等基因缺損之實體腫瘤,如乳癌、卵巢癌、胰臟癌及攝護腺癌等。此藥物具備成為新一代救援藥物的潛力,能抑制對現有 DDR 藥物產生抗藥性的腫瘤細胞。
圖(10)CX-5461(資料來源:生華科公司網站)
CX-4945 (Silmitasertib):蛋白激酶 CK2 抑制劑
CX-4945 為市場首見之蛋白激酶 CK2 抑制劑,透過抑制 CK2 蛋白激酶,干擾癌細胞 DNA 修復機制,調控多條致癌路徑,促使癌細胞凋亡,並增強 DNA 破壞藥物的殺傷力。CX-4945 主要開發用於膽管癌、髓母細胞瘤、基底細胞癌、膽道癌、神經母細胞瘤等罕見癌症。此藥物已取得美國 FDA 多項孤兒藥資格認定 (ODD) 及罕見兒科疾病認定(RPDD),享有臨床試驗支出抵稅、減免使用者費用及上市後 7 年市場獨賣期等法規優勢。此外,Silmitasertib 亦曾評估於社區型肺炎 (CAP] 之應用潛力,但在 2025 年 3 月因策略考量提前終止該二期臨床試驗收案。

圖(11)CX-4945(資料來源:生華科公司網站)
研發管線概況

圖(12)開發進程(資料來源:生華科公司網站)
生華科採取以臨床開發為主、基礎研究為輔的策略,研發管線涵蓋多種癌症類型,且臨床進展穩健。
| 藥物名稱 | 作用機制 | 主要適應症 | 臨床階段 (截至 2025 初) | 特殊認定 |
|---|---|---|---|---|
| CX-5461 [Pidnarulex) | G-四聯體穩定劑/RNA 聚合酶 I 抑制劑 | 血液性癌症、乳癌、卵巢癌、胰臟癌、攝護腺癌(尤其 BRCA2/PALB2 缺損) | Phase I (澳洲完成]、Phase I/II(加拿大乳癌進行中)、美國 NCI NExT 計畫支持多項合併用藥試驗(含免疫療法、ADC] | First-in-class |
| CX-4945 (Silmitasertib) | 蛋白激酶 CK2 抑制劑 | 膽管癌、髓母細胞瘤、基底細胞癌、膽道癌、神經母細胞瘤、復發/難治型兒童實體腫瘤 | Phase II(多國多中心進行中,含膽管癌、基底細胞癌、兒科腫瘤)、Phase I (基底細胞癌劑量延伸試驗完成,數據正向]、新冠肺炎 Phase II [已終止]、社區型肺炎 Phase II(已終止) | 美國 FDA 孤兒藥 (ODD]:膽管癌、髓母細胞瘤、神經母細胞瘤 美國 FDA 罕見兒科疾病 (RPDD]:髓母細胞瘤、神經母細胞瘤 |
| CX-8184 | (未揭露) | (臨床前) | 臨床前研究 | (未適用] |
產品應用領域與市場潛力
生華科產品線鎖定癌症治療及抗病毒感染 (策略調整後重心仍在癌症) 兩大領域,具備廣闊市場潛力:
腫瘤治療領域
-
血液性癌症與實體腫瘤:CX-5461 針對血液性癌症及多種實體腫瘤,特別是具 BRCA2/PALB2 基因缺損之癌症,符合精準醫療趨勢。
-
罕見癌症:CX-4945 鎖定膽管癌、髓母細胞瘤、基底細胞癌、神經母細胞瘤等罕見癌症,已取得多項美國 FDA 孤兒藥及罕見兒科疾病資格認定,具備市場獨賣期及法規優勢。全球罕見疾病藥物市場因政策利多及高價值特性,成為業界搶占焦點。
-
免疫療法:公司計畫於 2025 年跨足免疫療法藥物開發,聚焦癌症、發炎及自體免疫疾病。全球免疫療法市場預計至 2036 年將超過 1.58 兆美元,年複合成長率 (CAGR) 達 15.2%,市場前景可期。生華科將持續發展免疫療法市場,符合全球生技產業主流趨勢,並加速罕見疾病藥物 Silmitasertib(CX-4945)開發,預計加快上市腳步。
抗病毒感染領域
- 社區型肺炎 (CAP):CX-4945 曾展現抗病毒潛力,評估用於新冠/流感引發之社區型肺炎。然因 2025 年 3 月考量流感及新冠病毒感染高峰期已過,臨床收案困難,公司基於策略考量提前終止該二期臨床試驗收案,將資源聚焦於癌症領域。
營運與財務概況
圖(13)6492 生華科 營收趨勢圖呈現了公司營收的歷史變化。圖、6492 生華科 獲利能力則展示了公司的毛利率、營益率與純益率等獲利指標。
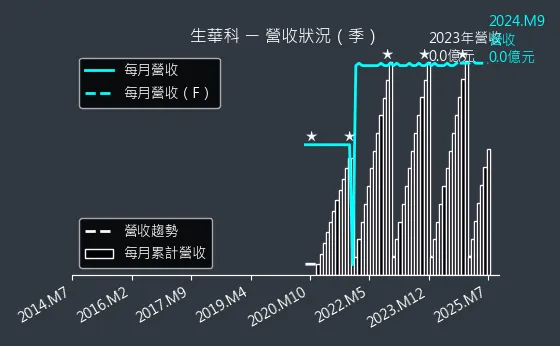
圖(14)6492 生華科 營收趨勢圖(本站自行繪製)
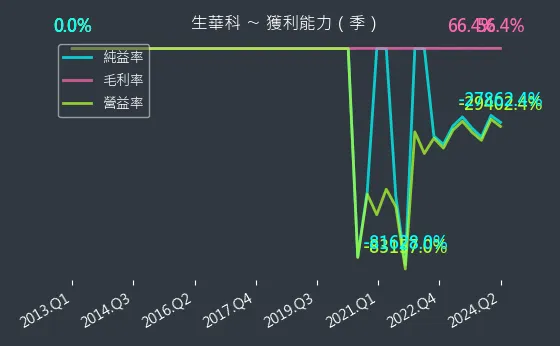
圖(15)6492 生華科 獲利能力(本站自行繪製)
營收結構與資本狀況
截至 2024 年底,生華科實收資本額約新台幣 8.97 億元,已發行股數約 8,974 萬股,市值約 37.96 億元。公司董監持股比例約 8.3%,外資持股約 4.48%。
目前公司營收主要來自於技術諮詢服務及研發合作相關勞務收入。由於新藥產品尚處於研發及臨床試驗階段,未有大量商業化產品上市,因此尚無具體產品銷售營收佔比數據。2025 年初,每月營收維持在約新台幣 8 萬多元的水平,2024 年全年累計營收約 100 萬元。
財務表現
生華科目前仍處於研發投入期,研發費用是主要成本支出。根據過往資訊,公司每年研發費用約新台幣 3.5 億元。雖然公司毛利率數據曾達 47.7% [主要來自技術服務),但因龐大的研發投入,整體獲利仍處於虧損狀態,近四季每股盈餘(EPS)為負數。公司表示,未來若有需要將適時辦理募資活動以確保研發推進,但近期 (截至 2025 年初] 無發債、現金增資或可轉換公司債計畫。公司營運資金主要來自自有資金、先前股權融資 (包含員工認股權及現金增資] 及國際合作機構贊助。
觀察公司財務結構,圖(16)6492 生華科 不動產、廠房、設備及待出售非流動資產變化圖顯示了公司非流動資產的變化;圖、6492 生華科 合約負債則呈現了公司的預收款項情況,可作為評估未來潛在訂單的參考。
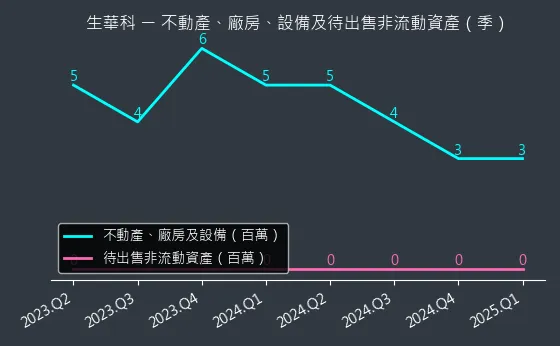
圖(17)6492 生華科 不動產、廠房、設備及待出售非流動資產變化圖(本站自行繪製)
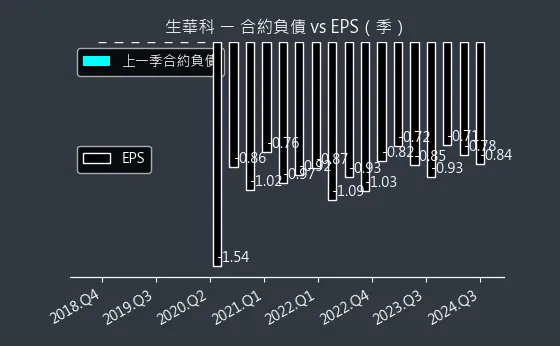
圖(18)6492 生華科 合約負債(本站自行繪製)
圖(19)6492 生華科 存貨與平均售貨天數及圖、6492 生華科 存貨與存貨營收比則分別呈現了公司的存貨狀況,有助於了解公司的庫存管理能力。
圖(20)6492 生華科 存貨與平均售貨天數(本站自行繪製)
圖(21)6492 生華科 存貨與存貨營收比(本站自行繪製)
圖(22)6492 生華科 現金流狀況提供了公司現金流量的資訊,而圖、6492 生華科 杜邦分析則展示了公司的財務狀況,可作為評估公司獲利能力的參考。圖、6492 生華科 資本結構則呈現了公司的資本來源。
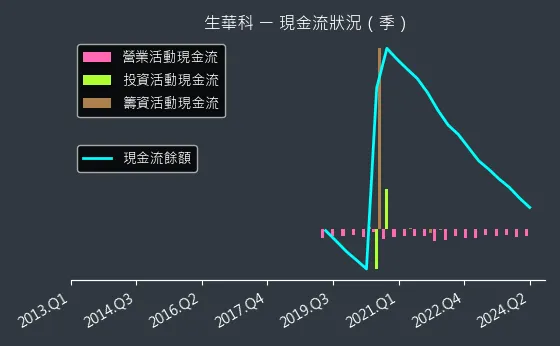
圖(23)6492 生華科 現金流狀況(本站自行繪製)
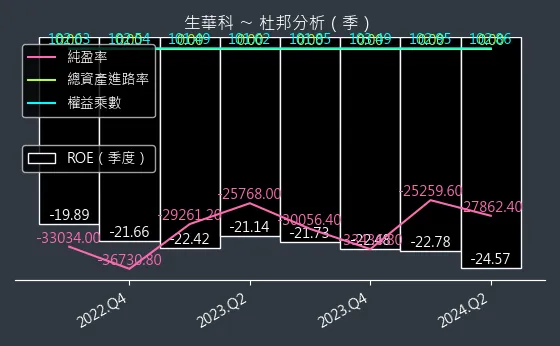
圖(24)6492 生華科 杜邦分析(本站自行繪製)
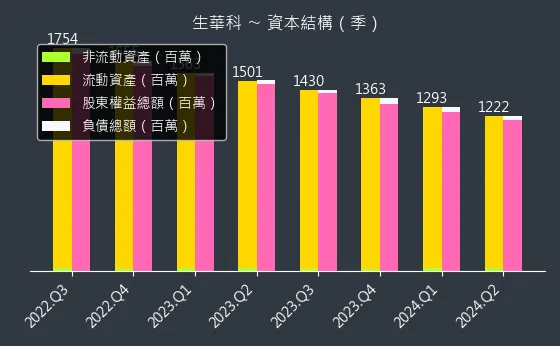
圖(25)6492 生華科 資本結構(本站自行繪製)
圖(26)6492 生華科 股利政策則呈現了公司的股利發放狀況。
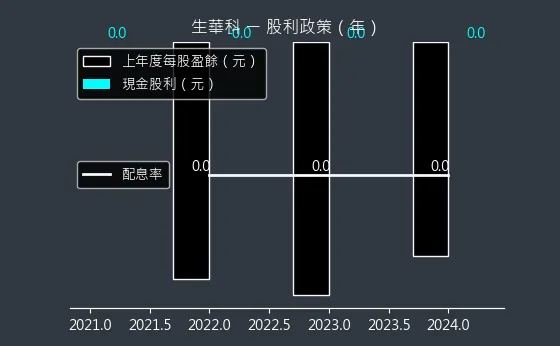
圖(27)6492 生華科 股利政策(本站自行繪製)
市場布局與競爭分析
生華科於 2024 年 4 月 2 日公告,新藥 CX-4945 治療基底細胞癌臨床試驗報告數據正向,將積極展開區域授權,加速 CX-4945 上市。試驗共收治 25 位局部晚期及轉移性晚期基底細胞癌患者,22 位可分析患者中,3 位局部晚期患者達部分緩解 [PR),10 位患者疾病穩定(SD),包含 2 位轉移性和 8 位局部晚期患者。轉移性和局部晚期患者疾病控制率分別為 80% 及 65%。局部晚期患者疾病無惡化存活期 [PFS] 中位數為 9.2 個月,轉移性晚期患者疾病無惡化存活期 [PFS) 中位數為 3.7 個月。局部晚期患者疾病控制期(DDC)中位數為 10.3 個月,轉移性晚期患者疾病控制期(DDC] 中位數為 7.5 個月。CX-4945 具長期使用的安全性,患者因副作用停藥率為 24%,且耐受性優於第一線療法 Hedgehog pathway inhibitors。公司將積極進行授權談判,並評估單劑或合併 Libtayo 治療。
全球市場布局策略
生華科以全球市場為目標,積極拓展國際合作,臨床試驗布局涵蓋:
-
美國:全球最大藥品市場,為生華科重點目標市場。已於美國展開多項臨床試驗 (CX-4945 兒科腫瘤、基底細胞癌等),並與美國國家癌症研究所 (NCI]、Banner Health、賓州州立大學附設兒童醫院等機構建立合作關係。
-
加拿大:進行 CX-5461 乳癌臨床試驗。
-
澳洲:完成 CX-5461 第一期臨床試驗。
-
台灣:曾獲准執行 CX-4945 抗新冠病毒二期臨床試驗 (後終止)。
未來產品上市後,預計銷售區域將涵蓋美國、歐洲及亞洲等主要醫療市場。
主要競爭對手
生華科於抗癌藥物市場面臨來自國內外藥廠之競爭。
台灣本土競爭對手 (小分子新藥領域):
-
美吾華 (1731)
-
寶齡富錦 (1760)
-
國鼎 (4132)
-
太景*-KY (4157)
-
智擎 (4162)
-
友霖 (4166)
-
泰宗 (4169)
-
因華 (4172)
-
杏國 (4192)
-
泰合 (6467)
國際大型藥廠競爭對手:
-
CX-5461 面臨 Novartis、Pfizer、Bristol-Myers Squibb、Roche、Johnson & Johnson 等大型藥廠相關抗癌藥物的競爭。
-
CX-4945 在膽管癌等領域則可能與 Eli Lilly、Bristol-Myers Squibb、Roche 等國際藥廠競爭。
圖(28)6492 生華科 法人籌碼(日)、圖、6492 生華科 大戶籌碼(週)與圖、6492 生華科 內部人持股(月)分別呈現了法人、大戶與內部人等籌碼動向。
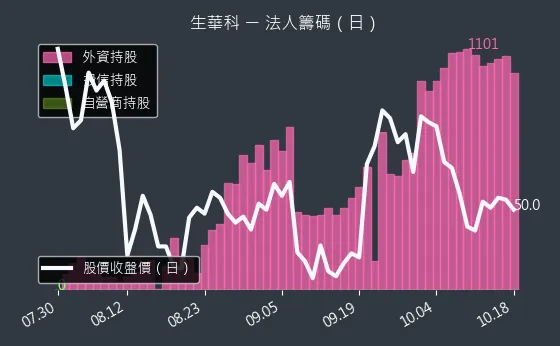
圖(29)6492 生華科 法人籌碼(日)(本站自行繪製)
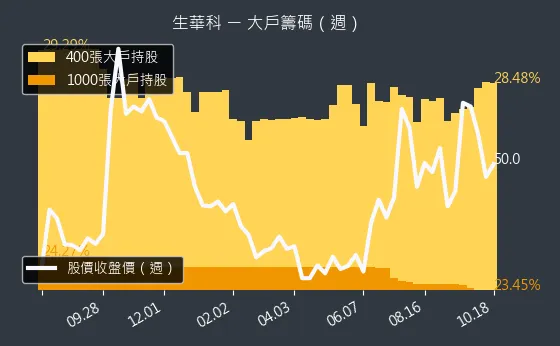
圖(30)6492 生華科 大戶籌碼(週)(本站自行繪製)
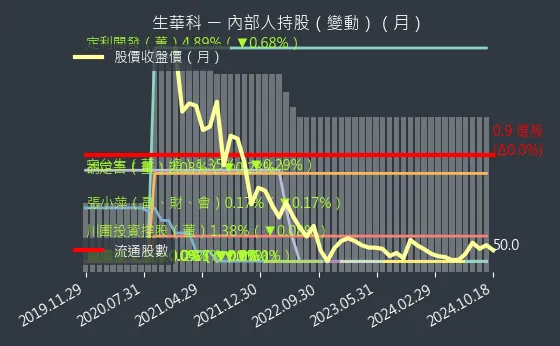
圖(31)6492 生華科 內部人持股(月)(本站自行繪製)
競爭優勢分析
生華科於競爭激烈的抗癌藥物市場中,具備以下核心競爭優勢:
-
創新研發能力與獨特機制:專注 First-in-class 新藥開發。CX-5461 為全球首個臨床運用 G-四鏈體作用機制的抗癌藥,具備抑制 DNA 損傷反應 (DDR) 的獨特機制,能克服抗藥性。CX-4945 為市場首見 CK2 抑制劑。
-
多適應症開發潛力:產品線涵蓋多種實體腫瘤、血液癌症及罕見疾病,具備「一藥多癌」潛力,符合精準醫療趨勢。
-
國際合作夥伴關係與認證:與美國國家癌症研究所 (NCI)、Beat Childhood Cancer Research Consortium(BCCRC)、國際藥廠 (如輝瑞] 等權威機構建立合作,提升研發實力與國際能見度。
-
孤兒藥與罕見兒科疾病資格認定:CX-4945 已獲美國 FDA 多項孤兒藥 (ODD) 及罕見兒科疾病(RPDD)資格認定,享有市場獨賣期、優先審查憑證 (PRV] 申請資格等法規優勢,降低開發成本與市場風險。
-
台灣生技領先地位與國際能見度:被歐洲媒體點名為 2025 年最受關注的台灣生技公司,為唯一進入美國國家隊 (NCI NExT 計畫) 的台灣生技企業,具備高度國際能見度。
近期重大事件與進展
生華科近期在新藥研發、臨床試驗及國際合作方面取得多項重要進展:
CX-5461 (Pidnarulex) 重要進展
-
NCI NExT 計畫贊助 [2024.09):獲美國國家癌症研究所(NCI)五年期贊助,支持其五年抗癌計畫實驗用藥。NCI 將主導 CX-5461 於晚期實體腫瘤患者之藥效動力學臨床試驗,並探索多種生物標記及擴大適應症開發,可能合併免疫療法、抗體藥物複合物(ADC] 等進行人體試驗。此利多消息曾激勵股價漲停至 52.3 元。
-
ESMO 年會發表 (2024.08-09):於 2024 年歐洲腫瘤醫學學會 (ESMO] 年會以海報形式發表 Phase 1b 臨床試驗結果摘要,數據由加拿大 Princess Margaret Cancer Centre 撰寫,顯示 Pidnarulex 對於治療帶有 BRCA2 或 PALB2 基因缺損之多種癌症具有治療潛力。
CX-4945 (Silmitasertib) 重要進展
-
基底細胞癌 [BCC) 數據正向與授權談判(2025.04):完成治療基底細胞癌 Phase I 人體臨床試驗 (收治 25 位局部晚期及轉移性晚期患者],數據分析結果正向。試驗對象為接受標準療法無效復發患者。22 位可分析患者中,3 位局部晚期患者達部分緩解 (PR],10 位疾病穩定(SD)。轉移性和局部晚期患者疾病控制率 [DCR] 分別為 80% 及 65%。局部晚期患者疾病無惡化存活期 [PFS] 中位數為 9.2 個月,轉移性晚期患者為 3.7 個月。局部晚期患者疾病控制期(DDC)中位數為 10.3 個月,轉移性晚期患者為 7.5 個月。部分患者 PFS 超過 21 個月 (最長 667 天]。CX-4945 展現較現行一、二線療法(如 Hedgehog pathway inhibitors)更好的耐受性(副作用停藥率 24%] 及疾病控制率。公司將積極進行區域授權談判,並評估單劑或合併 Libtayo 治療。
-
兒科腫瘤臨床試驗啟動 [2024.11):於美國賓州州立健康兒童醫院成功收治首位復發/難治型兒童及青少年實體腫瘤患者,展開 Phase II 臨床試驗。該試驗由全美知名的兒癌聯盟 Beat Childhood Cancer Research Consortium(BCCRC] 與賓州州立大學附設兒童醫院合作,計畫由 Dr. Giselle Saulnier Sholler 主導,利用全美超過 55 間醫院資源進行。試驗經費由 Four Diamonds Foundation 贊助,生華科提供新藥,初步規劃收治 59 位兒童,涵蓋神經母細胞瘤、尤因氏肉瘤和骨肉瘤等預後不良且醫療需求未滿足之病症。
-
神經母細胞瘤孤兒藥認定 (2024.10):獲美國 FDA 授予針對神經母細胞瘤的孤兒藥資格認定 (ODD]。若成為首個核准用於該適應症的藥物,將享有 7 年市場獨賣保護期。此為 CX-4945 繼膽管癌、髓母細胞瘤後再獲 ODD。
-
罕見兒科疾病認定 [RPDD):CX-4945 已獲得針對髓母細胞瘤及神經母細胞瘤的美國 FDA 罕見兒科疾病認定(RPDD),有助於爭取優先審核憑證(PRV],加速上市進程。
-
社區型肺炎試驗終止 (2025.03):因策略考量 (流感及新冠高峰已過,收案困難],提前終止 CX-4945 治療社區型肺炎之 Phase II 臨床試驗收案。
團隊與治理
-
延攬馮玉蓮博士 (2024.11):延攬具近 30 年國際藥廠研發經驗的馮玉蓮博士擔任法人董事代表,強化經營團隊專業能力。
-
董監酬金議題 (2025.01):媒體報導指出,生華科在虧損狀態下,2023 年度平均董監酬金達 103.34 萬元,較前一年增加 44.08 萬元,連續四年增加,引發市場關注。
市場與概念股連結
-
免疫療法題材 (2024.12):公司宣布將於 2025 年加速進入免疫療法藥物開發,符合全球生技產業主流趨勢。
-
熱門概念股:因其在抗癌新藥及罕見病藥物的創新研發、屢獲國際認證與合作,被視為台灣生技產業的熱門題材概念股。歐洲媒體評選為 2025 年 最受關注台灣生技公司。
-
疫情概念股關聯 (2025.01):曾因 CX-4945 抗病毒潛力被短暫歸類為疫情概念股,但隨著相關臨床試驗終止,關聯性已降低。
-
股價指數調整 (2025.02):被台灣指數公司自「特選上櫃生技醫療股價指數」成分股中刪除。
未來發展策略與展望
研發策略
-
聚焦核心產品:持續推進 CX-5461 及 CX-4945 的臨床試驗,特別是針對具 BRCA2/PALB2 基因缺損腫瘤、罕見癌症 (如基底細胞癌、兒科腫瘤) 等利基市場。
-
拓展免疫療法:於 2025 年 起加速布局免疫療法藥物開發,結合現有小分子藥物技術,開發新型免疫調節藥物,拓展癌症、發炎及自體免疫疾病治療領域。
-
深化精準醫療:利用生物標記等工具,提升藥物開發成功率與市場區隔。
市場策略
-
加速罕病新藥開發與上市:利用 CX-4945 已取得的多項 ODD 及 RPDD 資格,爭取優先審查,加快罕見病藥物上市腳步。
-
尋求國際授權與合作:針對臨床數據正向的產品 (如 CX-4945 於基底細胞癌),積極展開區域性或全球性授權談判,引進外部資源,分攤風險並加速商業化。
-
強化國際合作:持續與 NCI、BCCRC 等國際級研究機構及藥廠合作,擴大臨床試驗規模與範圍,提升全球市場能見度。
風險管理
-
多管線布局:維持多個臨床開發專案,分散單一藥物失敗風險。
-
資金管理:透過國際合作補助、孤兒藥政策優惠及未來可能的股權融資或授權收入,確保研發資金穩定。
-
策略調整彈性:如提前終止社區型肺炎試驗,展現依據市場與臨床狀況調整資源配置的彈性。
重點整理
-
創新研發驅動:生華科專注 First-in-class 小分子抗癌新藥,CX-5461 與 CX-4945 具備獨特作用機制與多重適應症潛力。
-
國際合作與認證加持:與 NCI、BCCRC 等國際機構深度合作,多項 ODD/RPDD 認定提供法規與市場優勢。
-
臨床進展顯著:CX-5461 獲 NCI 五年計畫支持;CX-4945 在基底細胞癌及兒科腫瘤試驗取得重要進展,數據正向。
-
聚焦精準醫療與罕見病:產品開發緊密結合 BRCA2/PALB2 等基因標記,並鎖定膽管癌、神經母細胞瘤等多種罕見癌症利基市場。
-
拓展免疫療法藍圖:計畫 2025 年 跨足高成長的免疫療法領域,拓展長期發展空間。
-
財務狀況:仍處研發投入期,營收有限,獲利為負,但透過合作與政策優惠管理資金需求。
-
市場高度關注:國際能見度高,被視為台灣生技產業指標性公司之一,具熱門題材概念股特性。
整體而言,生華生物科技憑藉其創新的研發管線、積極的國際合作策略及在精準醫療與罕見病領域的布局,已在全球生技產業中建立獨特定位。雖然公司仍處於研發投入階段,面臨新藥開發的固有風險,但其核心產品在臨床試驗中展現的潛力,以及未來在免疫療法領域的拓展,為公司長期發展奠定基礎,後續的臨床數據發布、授權談判進展及產品上市時程將是觀察重點。
參考資料說明
公司官方文件
-
生華生物科技股份有限公司公司基本資料
-
生華生物科技股份有限公司法人說明會簡報 (2024.12.26)
-
生華生物科技股份有限公司重要公告與新聞稿 (包含臨床試驗進展、合作案、認定資格等)
-
生華生物科技股份有限公司 109 年度現金增資發行新股公開說明書 (提及募資策略)
-
生華生物科技股份有限公司 2023 年股東會年報 (提及董監酬金)
產業研究報告
-
元大投顧產業分析報告 (2024.12)
-
富邦證券產業研究報告 (2024.12)
-
凱基證券投資分析報告 (2025.01)
-
國泰證券相關報告或法說會摘要 (提及參與法說會)
新聞報導
-
鉅亨網產業分析專文 (2024.12.27, 2024.09.21, 2024.09.12, 2024.08.04, 2025.02.18 等)
-
經濟日報專題報導 (2024.12.26, 2024.10.26, 2024.11.02 等)
-
工商時報產業分析 (2024.11.11, 2024.11.06 等)
-
GeneOnline 基因線上專題報導 (2024.09.18, 2025.03.07 等)
-
MoneyDJ 理財網新聞與 Wiki (2024.09.12, 2024.10.14, 公司基本資料, 競爭對手資訊等)
-
中央社新聞 (2024.11.06)
-
Yahoo! 股市新聞 (2024.09.21, 2024.10.25, 公司基本資料, 營收數據等)
-
環球生技月刊 [GBimonthly) 新聞(2024.09.09, 2024.08.07, 2025.03.29, 2025.04.02, 2024.10.26 等)9. 其他財經媒體報導 (如 Wantgoo、NStock、HiStock、StockFeel、CMoney、PressPlay、ETtoday、Scribd、Fugle、Winvest、StatementDog、Goodinfo 等提供之公司基本資料、營收、股價、新聞摘要、法人報告連結等]
永續發展文件
- 科學基礎減量目標倡議 [SBTi) 審核報告(2024.12)(此項於輸入資料提及,但與生華科關聯性待確認]
註: 本文內容主要依據 2023 年底至 2025 年初 之公開資訊進行分析與整理。所有財務數據、臨床試驗進展及市場分析均來自公開可得之官方文件、研究報告及新聞報導。部分資訊來源為 Perplexity AI 彙整提供。
